Bisolfito
Lo ione bisolfito (o, come raccomandato dalla nomenclatura IUPAC, idrogenotriossosolfito) è l'anione acido di zolfo HSO3−, con lo zolfo in stato di ossidazione +4.
I sali contenenti questo ione sono detti bisolfiti, o più correttamente (nomenclatura IUPAC) idrogenosolfiti.
Reazioni
modificaI sali idrogenosolfiti sono tipicamente preparati dal trattamento di una soluzione alcalina con eccesso di anidride solforosa, per esempio nel caso del bisolfito di sodio:
HSO3− è la base coniugata dell'acido solforoso, H2SO3:
L'acido solforoso non è un composto isolabile e non sembra esistere neanche in soluzione. Un equilibrio più reale rivelato con l'aiuto della spettroscopia è il seguente:
HSO3− è uno ione leggermente acido con una pKa di 6.97. È l'acido coniugato dello ione solfito, SO32−:
Struttura
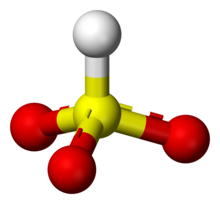
modificaLa maggior parte degli ioni bisolfito ha l'atomo di idrogeno collocato sull'atomo di zolfo, tuttavia alcuni esperimenti hanno dimostrato tramite la spettroscopia a risonanza magnetica nucleare che due tautomeri dell'idrogenosolfito coesistono in equilibrio, una avente simmetria C3v (protonato allo zolfo) ed un altro la simmetria Cs (protonato all'ossigeno).[1] La struttura C3v è supportata anche da diverse cristallografie a raggi X.
Note
modifica- ^ D. A. Horner, R. E. Connick, Inorg. Chem. 25, 2414-7 (1986).
Altri progetti
modifica- Wikizionario contiene il lemma di dizionario «bisolfito»
- Wikimedia Commons contiene immagini o altri file su bisolfito