Deferiprone
Il deferiprone è un principio attivo che agisce come ferrochelante; esso è indicato secondo l'RCP[2] nel trattamento dell'accumulo di ferro (emosiderosi) nei pazienti affetti da talassemia maggiore, quando la terapia con deferoxamina è controindicata o non adeguata.
| Deferiprone | |
|---|---|
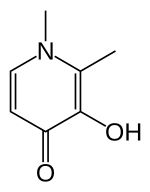 | |
| Nome IUPAC | |
| 3-idrossi-1,2-dimetilpiridin-4(1H)-one | |
| Nomi alternativi | |
| CP- 20 1,2-dimetil-3-hydroxyidrossi-4(1H)-piridinone 1,2-dimetil-3-idrossipirid-4-one 3-idrossi-1,2-dimetil-4(1H)- piridone 4(1H)-piridinone-1,2-dimetil-3-idrossi- 4(1H)-piridone,3-idrossi-1,2-dimetil-[1] | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C7H9NO2 |
| Massa molecolare (u) | 139.152 g/mol |
| Numero CAS | |
| Numero EINECS | 629-275-0 |
| Codice ATC | V03 |
| PubChem | 2972 |
| DrugBank | DBDB08826 |
| SMILES | O=C\1C(\O)=C(/N(/C=C/1)C)C |
| Dati farmacologici | |
| Categoria farmacoterapeutica | ferrochelante |
| Modalità di somministrazione | orale |
| Dati farmacocinetici | |
| Metabolismo | Coniugazione con Acido glicuronico |
| Emivita | 2-3 ore |
| Escrezione | renale dal 75% al 90%; metaboliti escreti: deferiprone libero, il metabolita glucuronide e il complesso ferro-deferiprone[2] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 - 315 - 319 - 335 |
| Consigli P | 261 - 305+351+338 [3] |
Il farmaco è stato studiato dalla ApoPharma[4]. In Italia è commercializzato dalla Chiesi Farmaceutici dal 1999, con il nome: Ferriprox.
Meccanismo d'azione
modificaIl principio attivo il deferiprone[5](3.idrossi-1,2.dimetilpiridina-4.one) che si comporta chimicamente come un antiossidante[1], è una molecola capace di legare il ferro in una proporzione molare di 3: 1. Monitorando la ferritina serica il deferiprone è capace di ridurre, prevenendolo, l'accumulo di ferro nei soggetti talassemici sottoposti a trasfusioni continue; pur non riducendo le lesioni agli organi interni.
Nei pochi studi effettuati il deferiprone si mostra meno efficace della deferossamina, per questo motivo è, rispetto a questa, una seconda scelta[6].
Sono stati pubblicati a tutto giugno 2010 più di 650 lavori che parlano di deferiprone; tra essi vi sono 4 metanalisi rilevanti:
- Deferasirox for the treatment of iron overload associated with regular blood transfusions (transfusional haemosiderosis) in patients suffering with chronic anaemia: a systematic review and economic evaluation[7]
- Oral deferiprone for iron chelation in people with thalassaemia[8]
- Desferrioxamine mesylate for managing transfusional iron overload in people with transfusion-dependent thalassaemia[9]
- Meta-analytic review of the clinical effectiveness of oral deferiprone (L1)[10]
Controindicazioni
modificaNon utilizzare in caso di gravidanza e allattamento, ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti; in caso di storia di neutropenia e/o precedenti di agranulocitosi, i pazienti non devono assumere medicinali noti come causa di neutropenia o potenzialmente in grado di causare l'agranulocitosi.
Effetti indesiderati
modificaSi possono manifestare artropatie, neutropenia, inoltre è notevole la diminuzione dello zinco nel corpo. Gli effetti collaterali più frequenti (con frequenza di 1/10) sono: nausea, dolore addominale, vomito e cromaturia (urine colorate). Con minore frequenza provoca: aumento degli enzimi epatici, neutropenia, agranulocitosi, emicrania, diarrea, artralgie, aumento dell'appetito, affaticamento.
Note
modifica- ^ a b ChemBank - Molecule Display, su chembank.broadinstitute.org. URL consultato il 9 luglio 2010.
- ^ a b FERRIPROX, su torrinomedica.it. URL consultato il 9 luglio 2010.
- ^ Sigma Aldrich; rev. del 27.07.2012
- ^ Ferriprox (deferiprone), su ferriprox.com. URL consultato il 9 luglio 2010.
- ^ www.ferriprox.com (PDF), su ferriprox.com. URL consultato il 9 luglio 2010 (archiviato dall'url originale l'8 novembre 2011).
- ^ Kontoghiorghes GJ, Neocleous K, Kolnagou A, Benefits and risks of deferiprone in iron overload in Thalassaemia and other conditions: comparison of epidemiological and therapeutic aspects with deferoxamine [collegamento interrotto], in Drug Safety : an International Journal of Medical Toxicology and Drug Experience, vol. 26, n. 8, 2003, pp. 553–84, PMID 12825969. URL consultato il 9 luglio 2010.
- ^ McLeod C, Fleeman N, Kirkham J, et al., Deferasirox for the treatment of iron overload associated with regular blood transfusions (transfusional haemosiderosis) in patients suffering with chronic anaemia: a systematic review and economic evaluation, in Health Technology Assessment (Winchester, England), vol. 13, n. 1, gennaio 2009, pp. iii–iv, ix–xi, 1–121, DOI:10.3310/hta13010, PMID 19068191. URL consultato il 9 luglio 2010 (archiviato dall'url originale il 26 luglio 2010).
- ^ Roberts DJ, Brunskill SJ, Doree C, Williams S, Howard J, Hyde CJ, Oral deferiprone for iron chelation in people with thalassaemia, in Cochrane Database of Systematic Reviews (Online), n. 3, 2007, pp. CD004839, DOI:10.1002/14651858.CD004839.pub2, PMID 17636775. URL consultato il 9 luglio 2010.
- ^ Roberts DJ, Rees D, Howard J, Hyde C, Alderson P, Brunskill S, Desferrioxamine mesylate for managing transfusional iron overload in people with transfusion-dependent thalassaemia, in Cochrane Database of Systematic Reviews (Online), n. 4, 2005, pp. CD004450, DOI:10.1002/14651858.CD004450.pub2, PMID 16235363. URL consultato il 9 luglio 2010.
- ^ Addis A, Loebstein R, Koren G, Einarson TR, Meta-analytic review of the clinical effectiveness of oral deferiprone (L1)., in Eur J Clin Pharmacol, vol. 55, n. 1, 1999, pp. 1-6, PMID 10206077.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su deferiprone